Autores: Yago Azevedo e Rhanoica Guerra
Editora: Ademilson Panunto-Castelo
Seminário apresentado junto ao Curso de Pós-Graduação em Imunologia Básica e Aplicada USP/RP
O artigo “Commensal-derived trehalose monocorynomycolate triggers γδ T cell-driven protective ocular barrier immunity”, publicado na revista “Immunity” (2026) por Xiaoyan Xu e colaboradores,1 demonstra que um glicolipídio derivado da bactéria comensal Corynebacterium mastitidis, denominado monocorinomicolato de trealose, induz uma resposta imunológica protetora mediada por células T γδ na superfície ocular, um tecido de barreira.
O equilíbrio entre o hospedeiro e as bactérias é essencial para a proteção contra patógenos, mas os fatores microbianos específicos responsáveis por modular essa imunidade ainda são pouco definidos. Nesse contexto, os autores investigaram como e quais componentes lipídicos de Corynebacterium mastitidis, integrante do microbioma ocular, contribuem para o estabelecimento de uma imunidade protetora no epitélio.
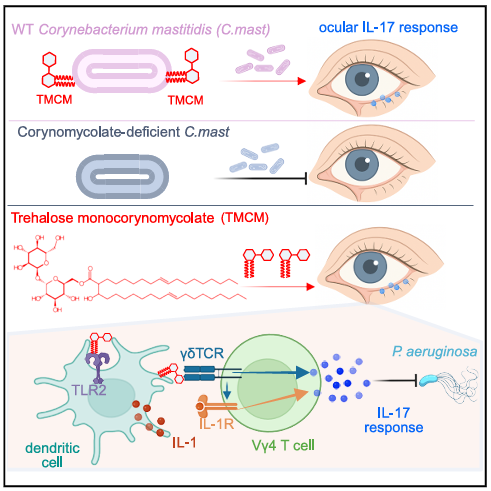
Inicialmente, foi demonstrado que extratos lipídicos da bactéria induzem a produção de IL-17 tanto in vitro, por células T γδ do subtipo Vγ4⁺ provenientes dos linfonodos cervicais, quanto in vivo. A análise lipidômica identificou que os ácidos micólicos de cadeia mais curta característicos de Corynebacterium, denominados corinomicolatos, especialmente os monocorinomicolatos conjugados à trealose (TMCM), são os principais responsáveis por essa atividade. De fato, a instilação ocular de C. mastitidis deficiente em corinomicolatos não induziu respostas de IL-17. Além disso, a utilização de TMCM sintético foi suficiente para reproduzir os efeitos da bactéria, confirmando seu papel como principal fator ativo.
Mecanisticamente, a ativação das células T γδ depende de interação célula-célula com células dendríticas (DCs). Nesse contexto, o TMCM atua como um ligante de receptores de reconhecimento de padrões (PRRs) nessas células. Especificamente, o TMCM é reconhecido por TLR2 e pelo receptor do tipo lectina C Mincle, expressos nas DCs, induzindo a produção de IL-1. Essa citocina é essencial para a ativação das células T γδ, uma vez que o bloqueio do receptor de IL-1 (IL-1R1) praticamente abole a produção de IL-17.
Embora os autores demonstrem que moléculas apresentadoras de antígeno, incluindo as do MHC (clássicas) e CD1d e MR1 (não clássicas), não são necessárias para a ativação das células T γδ, o engajamento do receptor de célula T (TCR) γδ mostrou-se fundamental para a produção de IL-17. Utilizando um modelo com deficiência na sinalização do TCR, observou-se redução significativa na expressão de IL-1R1 e IL-17 em resposta ao TMCM.
Funcionalmente, a aplicação tópica de TMCM promoveu o recrutamento de células T γδ produtoras de IL-17 e de neutrófilos para a conjuntiva, sem causar dano tecidual, caracterizando uma resposta protetora. Em modelos de infecção por Pseudomonas aeruginosa, o tratamento com TMCM reduziu significativamente a carga bacteriana, demonstrando seu papel na imunidade contra patógenos. Além disso, o efeito protetor do TMCM não se restringiu ao olho, sendo também observado em outros tecidos de barreira, como a pele e a mucosa oral.
Por fim, o estudo identifica o TMCM como o principal fator ativo de C. mastitidis, capaz de promover a ativação de células T γδ produtoras de IL-17, caracterizando um mecanismo dependente de células dendríticas, sinalização por IL-1 e engajamentodo TCR sinalização por IL-1 e engajamento do TCR. Esses achados destacam o potencial terapêutico do TMCM, inclusive como adjuvante, e revelam um novo mecanismo de imunidade de barreira envolvendo células T γδ.
Figura 1: O monocorinomicolato de trealose (TMCM), derivado de Corynebacterium mastitidis, é reconhecido por TLR2 em células dendríticas, induzindo a produção de IL-1. Essa citocina estimula a produção de IL-17 por células T γδ do subtipo Vγ4. Concomitantemente, a sinalização via TCR γδ é essencial para sustentar a expressão de IL-1R1 e potencializar a resposta dessas células, promovendo imunidade protetora contra patógenos. Fonte: Xiaoyan Xu et al., 2026.1
Referência
- Xu X, et al. Immunity, v.59, n.2, p.388-402, 2026. doi: 10.1016/j.immuni.2025.12.007.

- Apaixonados por Imunologia
- Comunicado
- Conteúdo Publicitário
- Curso
- Dept. Imunologia Clínica
- Dia da Imunologia
- Dia Internacional da Imunologia
- Divulgação científica
- Edital
- Especial
- Especial Dia da Imunologia
- Especial Doença de Chagas
- Evento
- Eventos
- Exposição COVID-19 da SBI
- História da Imunologia no Brasil
- Homenagem
- Immuno 2018
- Immuno2019
- Immuno2021
- Immuno2022
- Immuno2023
- Immuno2025
- Immuno2026
- IMMUNOLAC
- Immunometabolism2022
- Imune
- Imune - o podcast da SBI
- ImunoWebinar
- INCT Imuno
- Institucional
- IUIS
- Luto
- NeuroImmunology 2024
- Nota
- Nota Técnica
- Notícia
- o podcast da SBI
- Oportunidades
- Outros
- Parecer Científico
- Pesquisa
- Pint of Science 2019
- Pint of Science 2020
- Política Científica
- Sars-CoV-2
- SBI 50 ANOS
- SBI.ImunoTalks
- Sem categoria
- Simpósio
- SNCT 2020
- SNCT 2022
- Webinar
- WORKSHOP
.png)