Autores: Mahugnon Léger Erasme Gbaguidi e Stella Francy de Assunção
Editado por: Profa. Dra. Vanessa Carregaro
Referência: Cumpelik, A., Heja, D., Hu, Y. et al. (2021) Dynamic regulation of B cell complement signaling is integral to germinal center responses. Nature Immunology. 22:757–768. https://doi.org/10.1038/s41590-021-00926-0
O desenvolvimento de anticorpos direcionados a antígenos proteicos depende da apresentação do antígeno da célula B à célula T folicular. Tal processo induz a troca de classe do anticorpo, bem como a hipermutação somática de sua cadeia variável, afim de aumentar a afinidade do anticorpo pelo antígeno. Durante esse processo, frequentemente o anticorpo perde afinidade e recebe sinal de morte por células dendríticas foliculares e/ou células T foliculares. Entretanto, se houver aumento da afinidade, a célula B recebe sinal de sobrevivência. Dessa maneira, tais células passam novamente por hipermutação somática, caracterizando, assim, a seleção positiva, que ocorre no centro germinativo (CG) de maneira cíclica ao longo de semanas, processo denominado de maturação de afinidade.
Sabe-se que o sistema complemento apresenta um papel importante na ativação das células B por mecanismos que dependem da interação do correceptor do BCR, o CR2, à C3dg ligada à superfície de microrganismos. Alguns estudos com linfócitos T demonstram que o fator acelerador de decaimento (DAF – do inglês Decay Accelerating Factor) inibe a atividade de C3 convertase, reduzindo a sinalização mediada por C5aR e, por conseguinte, a função dessas células (Medof, 1984). Sabendo que a expressão do DAF está reduzida no centro germinativo, e que as células B expressam os receptores das anafilotoxinas C3a e C5a, foi levantada a questão acerca do papel imunomodulador da C3 convertase pelo DAF na ativação de células B.
Conforme esperado, a expressão de C3b está aumentada no CG de camundongos e de humanos, confirmando a atividade enzimática de C3 convertase elevada nesses sítios. No entanto, a expressão do inibidor do complexo de ataque à membrana, o CD59, também esteve aumentada nesse local. Porém, o receptor de C3b está reduzido, sugerindo, assim, que tanto a atividade de MAC, quanto a indução de apoptose estão inibidas no CG, apontando outra função para o aumento da atividade de C3 convertase. De modo interessante, observou-se um aumento inversamente proporcional na expressão de DAF e de BCL-6, fator de transcrição necessário para ativação das células B. Dessa forma, o grupo postulou que DAF poderia ser regulado por BCL-6, o que foi confirmado com uma análise de CHIP-seq. Nesse experimento foi demonstrado que BCL-6 estava presente na região de cromatina do DAF no centro germinativo de tonsilas humanas. Ainda, o tratamento com concentrações crescentes de BLC-6 inibiu, de maneira dose-dependente, a expressão de DAF em células de linhagem.
Em seguida, para determinar a função da C3 convertase na formação do CG, o grupo utilizou como ferramenta animais “DAF-TM”. Tais animais super-expressam o DAF em células B ativadas. Utilizaram também animais com deleção genética para os receptores C3aR1 e C5aR1 em células B ativadas. Observaram reduzida taxa proliferativa de células B no centro germinativo dos animais geneticamente modificados em comparação aos selvagens. Ainda, essa diminuição foi acompanhada pelo aumento da expressão de Caspase 3 e de receptores envolvidos na recirculação dos linfócitos B (CCR7 e S1P1). Conhecendo a relevância dos receptores C3aR1 e C5aR1 em células B ativadas, os autores investigaram o papel de tais receptores sobre o processo de hipermutação somática e, consequentemente, na maturação da afinidade. Foi avaliado, então a expressão do fator de transcrição MYC e do mTORC1, já descritos como essenciais para o processo de seleção positiva e maturação da afinidade de células B (Jellusova, 2020). Animais DAF-TM apresentam comprometimento na expressão destes fatores, bem como redução de anticorpos específicos e na frequência de hipermutação somática nas células B, sugerindo, assim, que a sinalização das anafilotoxinas em células B ativadas é necessária para que ocorra expressão de MYC e mTORC1 e, por conseguinte, a maturação da afinidade.
Assim, em conjunto, os dados apresentados evidenciam que o BCL-6 inibe a expressão de DAF por células B ativadas no centro germinativo. Esse processo favorece a atividade da C3 convertase, resultando em um acúmulo de C3a e de C5a. Ao se ligarem a seus receptores, as anafilotoxinas induzem a expressão de MYC e mTORC, promovendo a seleção positiva e maturação da afinidade pelas células B. Esta via de sinalização é importante também para a manutenção das células B no centro germinativo, mantendo sua taxa proliferativa e inibição da morte dessas células por apoptose dependente de Caspase 3 (Figura 1).
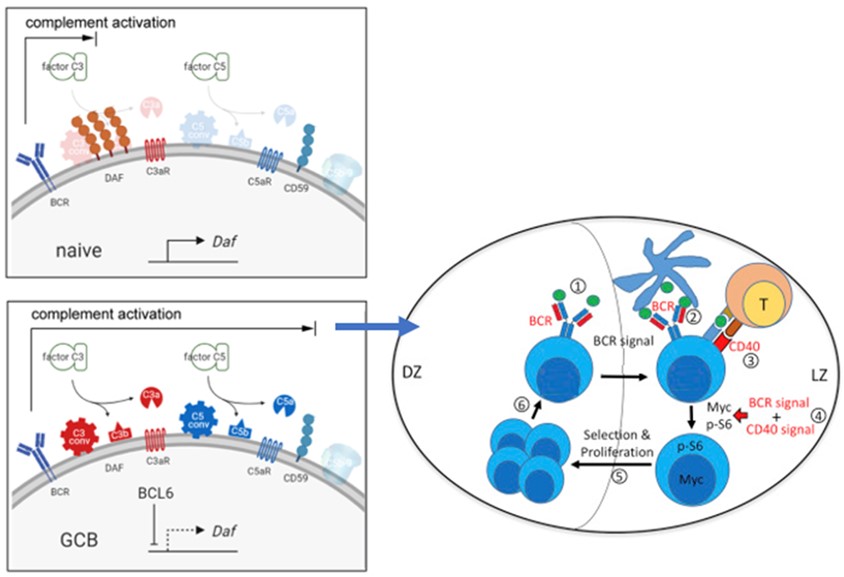
Figura 1 – Diagrama esquemático que ilustra os efeitos da ausência de DAF em produtos de ativação do complemento em células B no centro germinativo (topo) seguido pela via de sinalização complementar para a maturação da afinidade.
Referências
Jellusova, J., (2020) The role of metabolic checkpoint regulators in B cell survival and transformation. Immunological Reviews. 295:39–53.
Medof, M. E., Kinoshita, T., Nussenzweig, V., (1984) Inibição da ativação do complemento na superfície das células após a incorporação do fator acelerador de decaimento (FAD) em suas membranas. J. Exp. Med. 160 (5): 1558-1578.
Cumpelik, A., Heja, D., Hu, Y. et al. (2021) Dynamic regulation of B cell complement signaling is integral to germinal center responses. Nature Immunology. 22:757–768.

- Apaixonados por Imunologia
- Comunicado
- Conteúdo Publicitário
- Curso
- Dept. Imunologia Clínica
- Dia da Imunologia
- Dia Internacional da Imunologia
- Divulgação científica
- Edital
- Especial
- Especial Dia da Imunologia
- Especial Doença de Chagas
- Evento
- Eventos
- Exposição COVID-19 da SBI
- História da Imunologia no Brasil
- Homenagem
- Immuno 2018
- Immuno2019
- Immuno2021
- Immuno2022
- Immuno2023
- Immuno2025
- Immuno2026
- IMMUNOLAC
- Immunometabolism2022
- Imune
- Imune - o podcast da SBI
- ImunoWebinar
- INCT Imuno
- Institucional
- IUIS
- Luto
- NeuroImmunology 2024
- Nota
- Nota Técnica
- Notícia
- o podcast da SBI
- Oportunidades
- Outros
- Parecer Científico
- Pesquisa
- Pint of Science 2019
- Pint of Science 2020
- Política Científica
- Sars-CoV-2
- SBI 50 ANOS
- SBI.ImunoTalks
- Sem categoria
- Simpósio
- SNCT 2020
- SNCT 2022
- Webinar
- WORKSHOP
.png)










