Autores: Larissa Andrade e Thaílla Pacheco
Editora: Profa. Dra. Vanessa Carregaro
Seminário apresentado junto ao Curso de Pós-Graduação em Imunologia Básica e Aplicada da FMRP-USP.
Artigo intitulado “STAT5 and STAT3 balance shapes dendritic cell function and tumour immunity”.
As terapias antitumorais por bloqueio de pontos de verificação imunológicos (immune checkpoints blockade – ICB) atuam inibindo moléculas inibidoras como PD-1 e CTLA-4, que são expressas após a ativação dos linfócitos T para limitar sua resposta. [1]. Ainda que o uso de imunobiológicos seja considerado uma revolução na terapia antitumoral, a eficácia desta terapia pode ser comprometida por falhas na apresentação de antígenos, como perda de antígenos tumorais, defeitos na cadeia β da molécula de MHC ou ainda deficiência no processo de apresentação pelas células apresentadoras (APCs), como as células dendríticas (DCs). [2]
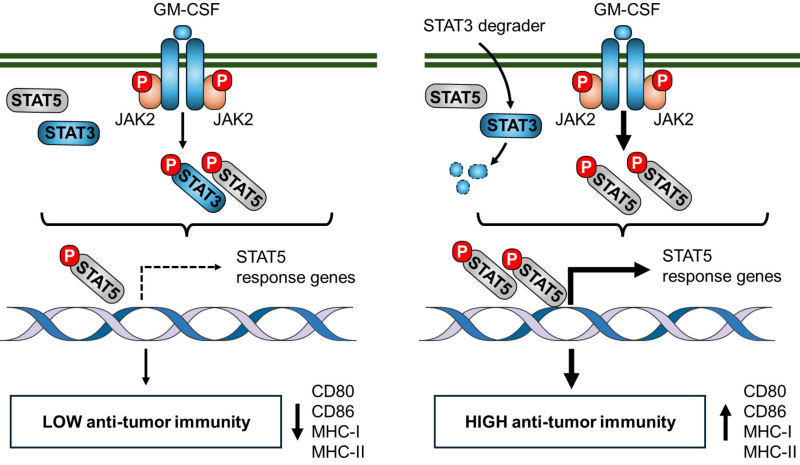
No contexto antitumoral, as células dendríticas convencionais tipo 1 (cDC1) são fundamentais para a eficácia da resposta imune. Vias de sinalização, como as mediadas por proteínas STAT, também influenciam essa resposta. [3] Sabe-se que a via da STAT3 possui uma função pró-tumoral, enquanto a via de STAT5 está associada à atividade antitumoral. [4,5]. Ambas podem ser ativadas via GM-CSF, que interage com seu receptor formado pelo heterodímero Gmrα-Gmrβ, desencadeando a ativação de JAK2 e a posterior fosforilação das proteínas STATs. [6] No entanto, a influência do equilíbrio entre STAT3 e STAT5 na resposta de DCs em associação com ICB ainda não era clara, e essa foi a questão que o trabalho de Zhou e colaboradores (2025) buscou responder. [7]
Utilizando uma coorte de pacientes com diversos tumores e tratados com diferentes terapias com imunobiológicos, o grupo verificou que existe associação entre a responsividade completa dos pacientes à ICB e à maior expressão de STAT5 em relação à STAT3. Experimentos in vitro demonstraram que a presença de STAT3 restringe a ativação de STAT5 via GM-CSF e JAK2 e reprime a expressão de genes associados à apresentação de antígenos e à produção de IL-12. Diante da indução do carcinoma de cólon (MC38), a deleção específica de Stat3 em cDC1 (Xcr1creStat3flox) resultou em melhora do prognóstico dos animais demonstrada pela redução do volume tumoral, bem como aumento da expressão de moléculas de MHC-I e II por cDC1 e maior assinatura efetora em linfócitos T CD8+ , evidenciada pela expressão de IFNγ, TNFα e perforinas.
O grupo mostra interesse no desenvolvimento de novas moléculas para associação com ICB e utilizou uma destas como indutora da degradação de STAT3 por meio da via ubiquitina-proteassoma, nomeada SD-36. O tratamento de cDC1 com SD-36, seguido de estímulo com LPS, aumentou a expressão de MHC, CD80 e CD86; o mesmo foi demonstrado in vivo em que, após inoculação de diferentes células tumorais (4T1 – câncer de mama, LLC – carcinoma de pulmão de Lewis e MC38) em camundongos selvagens, SD-36 reduziu o volume tumoral e a ocorrência de metástase. Essa melhora na resposta antitumoral foi atribuída à ativação de linfócitos T CD8+, evidenciada por maior produção IFNγ, TNFα e perforinas após o tratamento para degradação de STAT3, efeito abolido em camundongos Rag1-/- ou tratados com anticorpos anti-CD8. Por fim, os autores apresentaram a nova molécula SD-2301, com melhorias nos perfis farmacocinético e farmacodinâmico, que apresentou potencial terapêutico semelhante à molécula SD-36.
Dessa maneira, Zhou e colaboradores trazem a possibilidade de associação de terapias que modulem a expressão de STAT3 e as ICB, com foco no potencial uso em tumores metastáticos.
Figura 1. Zhou e colaboradores demonstraram que, no contexto tumoral, a via GM-CSF/JAK2 ativa, preferencialmente, STAT3, que culmina na transcrição de genes associados à resposta pró-tumoral, como IL-6 e IL-10. Ao utilizar o tratamento com SD-36 ou SD-2301, há degradação de STAT3, o que possibilita o favorecimento da ativação da via STAT5, induzindo a expressão de moléculas de MHC-I e II, CD80 e CD86, bem como maior papel efetor de linfócitos T CD8+.
Referências
[1] Wykes, M., Lewin, S. Immune checkpoint blockade in infectious diseases. Nat Rev Immunol 18, 91–104 (2018). https://doi.org/10.1038/nri.2017.112
[2] Zhou X, Ni Y, Liang X, Lin Y, An B, He X, Zhao X. Mechanisms of tumor resistance to immune checkpoint blockade and combination strategies to overcome resistance. Front Immunol. 2022 Sep 15;13:915094. doi: 10.3389/fimmu.2022.915094
[3] Li YJ, Zhang C, Martincuks A, Herrmann A, Yu H. STAT proteins in cancer: orchestration of metabolism. Nat Rev Cancer. 2023 Mar;23(3):115-134. doi: 10.1038/s41568-022-00537-3. Epub 2023 Jan 3. PMID: 36596870.
[4] Johnson, D., O'Keefe, R. & Grandis, J. Targeting the IL-6/JAK/STAT3 signalling axis in cancer. Nat Rev Clin Oncol 15, 234–248 (2018). https://doi.org/10.1038/nrclinonc.2018.8
[5] Zhou, J., Kryczek, I., Li, S. et al. The ubiquitin ligase MDM2 sustains STAT5 stability to control T cell-mediated antitumor immunity. Nat Immunol 22, 460–470 (2021). https://doi.org/10.1038/s41590-021-00888-3
[6] Liao, W., Lin, JX., Wang, L. et al. Modulation of cytokine receptors by IL-2 broadly regulates differentiation into helper T cell lineages. Nat Immunol 12, 551–559 (2011). https://doi.org/10.1038/ni.2030
[7] Zhou, J., Tison, K., Zhou, H. et al. STAT5 and STAT3 balance shapes dendritic cell function and tumour immunity. Nature 643, 519–528 (2025). https://doi.org/10.1038/s41586-025-09000-3
- Apaixonados por Imunologia
- Comunicado
- Conteúdo Publicitário
- Curso
- Dept. Imunologia Clínica
- Dia da Imunologia
- Dia Internacional da Imunologia
- Divulgação científica
- Edital
- Especial
- Especial Dia da Imunologia
- Especial Doença de Chagas
- Evento
- Eventos
- Exposição COVID-19 da SBI
- História da Imunologia no Brasil
- Homenagem
- Immuno 2018
- Immuno2019
- Immuno2021
- Immuno2022
- Immuno2023
- Immuno2025
- Immuno2026
- IMMUNOLAC
- Immunometabolism2022
- Imune
- Imune - o podcast da SBI
- ImunoWebinar
- INCT Imuno
- Institucional
- IUIS
- Luto
- NeuroImmunology 2024
- Nota
- Nota Técnica
- Notícia
- o podcast da SBI
- Oportunidades
- Outros
- Parecer Científico
- Pesquisa
- Pint of Science 2019
- Pint of Science 2020
- Política Científica
- Sars-CoV-2
- SBI 50 ANOS
- SBI.ImunoTalks
- Sem categoria
- Simpósio
- SNCT 2020
- SNCT 2022
- Webinar
- WORKSHOP
.png)