Autoras: Amanda de M. Becerra e Gabriélly B. Trindade
Editor: Ademilson Panunto Castelo
Seminário apresentado junto ao Curso de Pós-Graduação em Imunologia Básica e Aplicada da FMRP-USP
Em um estudo intitulado “Bacterial immunotherapy leveraging IL-10R hysteresis for both phagocytosis evasion and tumor immunity revitalization”, publicado no periódico Cell, em março de 2025, Zhiguang Chang1 e cols. investigaram como a imunoterapia com determinada cepa de bactéria bioengenheirada induzia a produção de interleucina 10 (IL-10) em tumores sólidos, promovendo um fenômeno denominado de histerese, que regula positivamente a expressão do receptor de IL-10 (IL-10R) em células do microambiente tumoral, contribuindo para o controle do crescimento e metástase do tumor.
A imunoterapia tem revolucionado o tratamento do câncer ao potencializar a resposta do sistema imunológico contra células tumorais. No entanto, a eficácia desses tratamentos pode ser limitada pelo microambiente tumoral, que frequentemente promove a imunossupressão e dificulta a ação das células do sistema imunológico. A IL-10 é tradicionalmente reconhecida por seu papel imunossupressor nesse contexto, inibindo a atividade dos linfócitos T e favorecendo a progressão tumoral.2
No entanto, estudo recente3 mostrou que a IL-10 também pode exercer efeitos benéficos, especialmente na ativação e manutenção da função das células T CD8+ dentro do tumor. Neste estudo, os autores exploraram uma imunoterapia com cepa de Salmonella enterica sorotipo Typhimurium, denominada de Designer Bacteria 1 (DB1), cujas modificações genéticas permitiram sua proliferação exclusivamente em ambientes anaeróbicos (com o gene asd sob o controle do promotor Phypo, suprimido por oxigênio) e a evasão dos vacúolos após a fagocitose (com o gene que codifica a listeriolisina O sob o controle de PsseA, um promotor induzido por sinais intravacuolares).
Inicialmente, os autores mostraram que o tratamento de camundongos portadores de tumores sólidos com DB1 promovia a localização e o crescimento das bactérias dentro desses tumores, enquanto elas desapareciam dos outros tecidos. Além disso, o tratamento inibiu significativamente o crescimento e as metástases do tumor, com sobrevida dos animais por todo período de observação. Mais importante ainda, nesse estudo foi mostrado que a eficácia do tratamento com DB1 está intrinsecamente ligada à memória imunológica específica para antígenos tumorais, prevenindo a recorrência e as metástases do tumor. Essa memória é advinda de células T CD8+ com fenótipo semelhante à memória e exaustão (CD62L−CD69+PD-1+TIM-3+), preexistentes no microambiente tumoral, as quais são ativadas e expandidas pela sinalização com IL-10. De fato, a IL-10 é responsável pela indução do aumento da expressão do IL-10R em linfócitos T CD8+ no início do desenvolvimento tumoral. Isso leva ao fenômeno da histerese, que reflete a dependência do histórico em sistemas físicos, o que significa que o sistema não retorna completamente ao seu estado original quando a estimulação diminui, resultando em um atraso nas concentrações de equilíbrio, como no caso do IL-10R. A IL-10 produzida pelo tratamento com DB1, estabelece um ciclo de feedback positivo que direciona as células dos sistema imunológico infiltrantes para um estado de alta expressão do IL-10R (IL-10Rhi).
Os macrófagos associados ao tumor foram identificados como uma fonte crucial de IL-10, cuja produção é estimulada pelo reconhecimento das bactérias presentes na imunoterapia, via receptor 4 similar a Toll (TLR4). Essa produção de IL-10 é fundamental tanto para ativar as células T CD8+ intratumorais quanto para regular a migração e a atividade fagocitária dos neutrófilos associados ao tumor, impedindo que destruam as bactérias no ambiente tumoral. Tal fato favorece a eficácia da terapia de forma localizada, contribuindo para a eliminação apenas das bactérias que alcançam tecidos saudáveis.
A terapia baseada em DB1 oferece vantagens significativas, como a administração intravenosa e a liberação contínua e localizada de IL-10 no tumor, superando barreiras sistêmicas. Além disso, a expressão de IL-10R em tumores pode servir como um indicador prognóstico valioso para terapias relacionadas à IL-10 ou terapias bacterianas. Essa abordagem representa um avanço promissor na compreensão e no tratamento de tumores sólidos, destacando a importância da modulação do microambiente tumoral para a eficácia terapêutica.
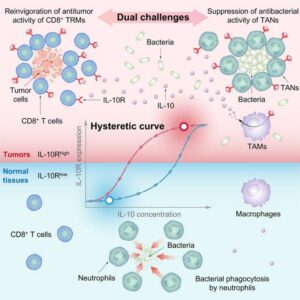
A sinalização IL-10/IL-10R desempenham um papel duplo na imunoterapia bacteriana, estimulando tanto a ativação da resposta antitumoral quanto a supressão da atividade antibacteriana. No microambiente tumoral, a IL-10 induz a expressão elevada de IL-10R (IL-10Rhi) em células T CD8+ residentes de memória (TRMs) e permite a reativação da resposta antitumoral. Por outro lado, IL-10 regula a atividade antimicrobiana dos neutrófilos associados a tumores (TANs), favorecendo a persistência bacteriana localmente. A curva de histerese da expressão de IL-10R demonstra como a exposição contínua à IL-10, mesmo que em baixos níveis, mantém a expressão do receptor nos tumores, contrastando com a menor expressão em tecidos normais (IL-10Rlo). Os macrófagos associados ao tumor (TAMs) são uma fonte crucial de IL-10, enquanto os neutrófilos desempenham um papel na fagocitose bacteriana nos tecidos saudáveis. Dessa forma é alcançado o equilíbrio entre resposta imunológica e controle da proliferação bacteriana no microambiente tumoral.
Referências
- CHANG, Z. et al. Bacterial immunotherapy leveraging IL-10R hysteresis for both phagocytosis evasion and tumor immunity revitalization. Cell, 2025. doi: 10.1016/j.cell.2025.02.002.
- LI, M. O.; FLAVELL, R. A. Contextual regulation of inflammation: a duet by transforming growth factor-beta and interleukin-10. Immunity, v.28, n.4, p.468-476, 1 abr. 2008. doi: 10.1016/j.immuni.2008.03.003.
- Zhao, Y., Chen, J., Andreatta, M. et al. IL-10-expressing CAR T cells resist dysfunction and mediate durable clearance of solid tumors and metastases. Nat Biotechnol, v.42, p.1693-1704, 2024. doi: 10.1038/s41587-023-02060-8
- Apaixonados por Imunologia
- Comunicado
- Conteúdo Publicitário
- Curso
- Dept. Imunologia Clínica
- Dia da Imunologia
- Dia Internacional da Imunologia
- Divulgação científica
- Edital
- Especial
- Especial Dia da Imunologia
- Especial Doença de Chagas
- Evento
- Eventos
- Exposição COVID-19 da SBI
- História da Imunologia no Brasil
- Homenagem
- Immuno 2018
- Immuno2019
- Immuno2021
- Immuno2022
- Immuno2023
- Immuno2025
- Immuno2026
- IMMUNOLAC
- Immunometabolism2022
- Imune
- Imune - o podcast da SBI
- ImunoWebinar
- INCT Imuno
- Institucional
- IUIS
- Luto
- NeuroImmunology 2024
- Nota
- Nota Técnica
- Notícia
- o podcast da SBI
- Oportunidades
- Outros
- Parecer Científico
- Pesquisa
- Pint of Science 2019
- Pint of Science 2020
- Política Científica
- Sars-CoV-2
- SBI 50 ANOS
- SBI.ImunoTalks
- Sem categoria
- Simpósio
- SNCT 2020
- SNCT 2022
- Webinar
- WORKSHOP
.png)