Por: Patrick Fernandes e Aline Carvalho (doutorandos IBA-FMRP/USP)
Editora: Luciana Benevides
As doenças cardiovasculares são a principal causa de morte nas últimas décadas, segundo dados da OMS e da Universidade de Oxford. A principal doença cardiovascular é a aterosclerose (1), caracterizada como uma doença crônica inflamatória ocasionada pelo acúmulo de colesterol LDL no sangue, o qual é retido na parede dos vasos. Não só o LDL se acumula na região dos vasos como também induz o influxo de monócitos inflamatórios que se diferenciam em macrófagos. Os macrófagos, ao fagocitarem altos níveis de LDL, tendem a se tornar células espumosas e morrem nos vasos iniciando reações inflamatórias levando à formação da placa lipídica. O rompimento da placa é ditado pela atuação do sistema imune adaptativo por meio das células Th1 que secretam IFN-gamma. As células Th17 possuem efeito protetor e as células T reguladoras (Tregs) inibem o papel inflamatório da Th1 (1). Caso a placa se rompa, o trombo pode obstruir vasos coronarianos e levar ao infarto do miocárdio.
Além dos fatores de risco para desenvolvimento de doenças cardíacas, como estilo de vida, alimentação e predisposição genética, estudos vêm mostrando como a privação de sono também pode comprometer a nossa saúde (2) e aumentar o risco de desenvolvimento de doenças cardíacas (3), além de doenças como câncer (4), diabetes tipo 2 (5), obesidade (6), etc. Em suma, a literatura mostra a importância do sono para prevenção do desenvolvimento de doenças cardiovasculares.
Para entender se o sono poderia regular e proteger de doenças cardíacas, um trabalho publicado recentemente na Nature (7) utilizou camundongos com predisposição genética para o desenvolvimento de aterosclerose. Esses animais foram submetidos a uma dieta rica em gordura e a um regime de fragmentação do sono, no qual eram acordados a cada dois minutos durante dezesseis semanas. Os camundongos que tinham o sono perturbado desenvolviam maiores lesões vasculares e apresentavam maior número de macrófagos inflamatórios na região dos vasos e na circulação sanguínea. Ao analisar a medula óssea, os camundongos com o sono fragmentado tinham maior quantidade de células que dão origem aos monócitos inflamatórios, além delas apresentarem maior atividade proliferativa.
É conhecido que perturbações no sono podem desencadear alterações nos níveis de alguns neurotransmissores. E a hipocretina, um neurotransmissor responsável, dentre outras coisas, pelo estado de vigília, tinha sua produção significantemente reduzida no hipotálamo de camundongos que foram submetidos a fragmentação do sono. A redução de hipocretina tinha relação direta com o aumento de monócitos inflamatórios na circulação sanguínea e da proliferação de progenitores na medula óssea. No entanto, ainda não era possível concluir que a redução da hipocretina causava o aumento da proliferação dessas células, uma vez que as células progenitoras de monócitos não apresentavam receptores para a hipocretina e não respondiam diretamente a ela in-vitro. Apesar de não apresentarem receptores de hipocretina, as células progenitoras de monócitos são sensíveis a estimulação com o fator estimulante de colônia de macrófagos (Csf1), que induzem a sua proliferação. Os pré-neutrófilos, células progenitores e imaturas da medula óssea, estão próximas a diversas outras subpopulações progenitoras, e apresentam na sua superfície receptores para a hipocretina. Os pré-neutrófilos, quando estimulados com hipocretina, reduzem a secreção de Csf1, e isso reduz a proliferação de células progenitoras de monócitos, ligando todos os pontos desse eixo de regulação (Figura 1).
Há mais de duas décadas é notório que o aumento de células circulantes do sistema imunológico está relacionado com o agravamento do quadro de aterosclerose, e os autores do recente trabalho demonstraram que noites de sono inadequadas podem resultar no aumento de monócitos inflamatórios circulantes que aumentam a inflamação local.
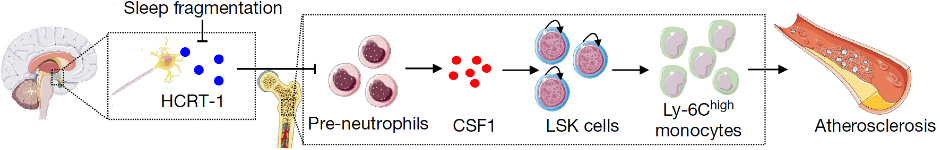
Figura 1 - A fragmentação do sono inibe a produção da hipocretina. A hipocretina é responsável pela inibição da produção de CSF1 por pré-neutrófilos. Na ausência de hipocretina os pré-neutrófilos produzem maiores quantidades de CSF1 que estimulam células progenitoras de monócitos a se proliferar e diferenciar em monócitos inflamatórios. Na circulação sanguínea os monócitos inflamatórios se depositam nos vasos para fagocitar o LDL e aumentam as placas de ateroma.
Referências
- Gisterå, A., Hansson, Göran K. The immunology of atherosclerosis. Nature Reviews Nephrology. 2017/04/10/online. Vol 13. 368. Nature Publishing Group, a division of Macmillan Publishers Limited. All Rights Reserved. 10.1038/nrneph.2017.51. Review Article (2017).
- Hafner, M., Stepanek, M., Taylor, J., Troxel, W. M. & van Stolk, C. Why sleep matters—the economic costs of insufcient sleep: a cross-country comparative analysis. Rand Health Q. 6, 11 (2017).
- Cappuccio, F. P., Cooper, D., D’Elia, L., Strazzullo, P. & Miller, M. A. Sleep duration predicts cardiovascular outcomes: a systematic review and meta-analysis of prospective studies. Eur. Heart J. 32, 1484–1492 (2011).
- Blask, D. E. Melatonin, sleep disturbance and cancer risk. Sleep Med. Rev. 13, 257–264 (2009).
- Shan, Z. et al. Sleep duration and risk of type 2 diabetes: a meta-analysis of prospective studies. Diabetes Care 38, 529–537 (2015).
- Cappuccio, F. P. et al. Meta-analysis of short sleep duration and obesity in children and adults. Sleep 31, 619–626 (2008).
- MCALPINE, C. S.; et al. Sleeps modulates haematopoiesis and protects against atherosclerosis. Nature, v. 556, p. 383–387, 2019.

- Apaixonados por Imunologia
- Comunicado
- Conteúdo Publicitário
- Curso
- Dept. Imunologia Clínica
- Dia da Imunologia
- Dia Internacional da Imunologia
- Divulgação científica
- Edital
- Especial
- Especial Dia da Imunologia
- Especial Doença de Chagas
- Evento
- Eventos
- Exposição COVID-19 da SBI
- História da Imunologia no Brasil
- Homenagem
- Immuno 2018
- Immuno2019
- Immuno2021
- Immuno2022
- Immuno2023
- Immuno2025
- Immuno2026
- IMMUNOLAC
- Immunometabolism2022
- Imune
- Imune - o podcast da SBI
- ImunoWebinar
- INCT Imuno
- Institucional
- IUIS
- Luto
- NeuroImmunology 2024
- Nota
- Nota Técnica
- Notícia
- o podcast da SBI
- Oportunidades
- Outros
- Parecer Científico
- Pesquisa
- Pint of Science 2019
- Pint of Science 2020
- Política Científica
- Sars-CoV-2
- SBI 50 ANOS
- SBI.ImunoTalks
- Sem categoria
- Simpósio
- SNCT 2020
- SNCT 2022
- Webinar
- WORKSHOP
.png)










