Autores: Jonatan Carvalho e Keise Adrielle Pereira
Editor: Prof. Dr. Ademilson Panunto Castelo
Seminário apresentado na disciplina Tópicos Avançados de Imunologia do Programa de Pós-Graduação em Imunologia Básica e Aplicada da FMRP-USP
Um estudo recente, intitulado “Influenza hijacks myeloid cells to inflict type-I interferon-fueled damage in the heart”, publicado na revista Immunity em fevereiro de 2026, por Jeffrey Downey e colaboradores,1 traz avanços importantes ao revelar que o vírus da Influenza A (Alphainfluenzavirus influenzae) não apenas afeta os pulmões, mas pode alcançar o coração e contribuir para o lesão cardíaca.
A infecção pelo vírus da Influenza A é amplamente reconhecida por causar doença respiratória aguda. Contudo, dados clínicos mostram, há décadas, um aumento nos casos de complicações cardiovasculares, como miocardite, insuficiência cardíaca e infarto, durante os surtos de gripe. Apesar dessa associação clínica bem estabelecida, os mecanismos biológicos que conectam uma infecção pulmonar ao comprometimento do miocárdio permaneciam pouco compreendidos.2
Para compreender esses mecanismos, os Downey e cols.1 analisaram, inicialmente, relatórios de autópsias de pacientes que morreram durante infecção pelo vírus da Influenza A. Esses registros mostraram que a maioria dos indivíduos apresentava comorbidades cardiovasculares e sinais de comprometimento cardíaco, incluindo alterações estruturais do miocárdio e marcadores de lesão cardíaca. Em paralelo, dados clínicos de pacientes hospitalizados indicaram que muitos desenvolvem elevação de biomarcadores séricos de lesão miocárdico, como a troponina. Esses achados reforçam a relevância clínica da interação entre a infecção viral e a saúde cardiovascular.
Em modelos experimentais, os pesquisadores demonstraram, por meio da dosagem de biomarcadores cardíacos e da ressonância magnética, que a infecção respiratória por influenza desencadeia inflamação no coração e comprometimento da função cardíaca, mesmo quando o vírus infecta inicialmente o pulmão. Em seguida, utilizando citometria de fluxo, rastreamento de linhagem e transcriptômica de célula única, os autores identificaram que o infiltrado cardíaco é dominado por uma população específica de células mieloides CD319⁺ derivadas de progenitores monócito-dendríticos (pró-DC3), e não por monócitos inflamatórios clássicos.
Uma das descobertas mais interessantes do trabalho foi o mecanismo pelo qual o vírus chega ao coração. Experimentos de parabiose demonstraram que partículas virais podem ser transportadas pela circulação no interior de células mieloides infectadas. Essas células são recrutadas ao miocárdio por um gradiente quimiotático envolvendo CCL2 e seu receptor CCR2, permitindo que transportem o vírus do pulmão ao miocárdio.
Uma vez no coração, o vírus se replica predominantemente em cardiomiócitos, e não nas células pró-DC3. Experimentos in vitro demonstraram que cardiomiócitos são permissivos à replicação viral, enquanto monócitos e macrófagos não apresentam essa capacidade. Imagens de imunofluorescência confirmaram a presença de cardiomiócitos infectados no miocárdio e sua proximidade com células CD319⁺. Além disso, ensaios de cocultura mostraram que essas células mieloides podem transferir o vírus para os cardiomiócitos, levando ao aumento da replicação viral e à liberação de marcadores de lesão cardíaca.
Outro achado relevante refere-se ao papel da sinalização por interferon do tipo I (IFN-I). Embora essa via seja essencial para o controle antiviral no pulmão, o estudo mostrou que, no coração, a ativação do receptor IFNAR1 em cardiomiócitos pode contribuir para inflamação e disfunção cardíaca. Utilizando tecnologia CRISPR-Cas9 para reduzir a expressão de IFNAR1 especificamente no coração, os autores observaram menor lesão miocárdica e melhor preservação da função cardíaca após infecção pelo vírus da Influenza A, quando comparado a camundongos controle infectados.
Em conjunto, os resultados revelam um mecanismo até então pouco conhecido: células do sistema imunológico atuam como veículos biológicos que transportam o vírus da Influenza A do pulmão ao miocárdio, permitindo que cardiomiócitos se tornem alvos da infecção. A resposta antiviral mediada por IFN-I, embora protetora no pulmão, pode tornar-se prejudicial no miocárdio.
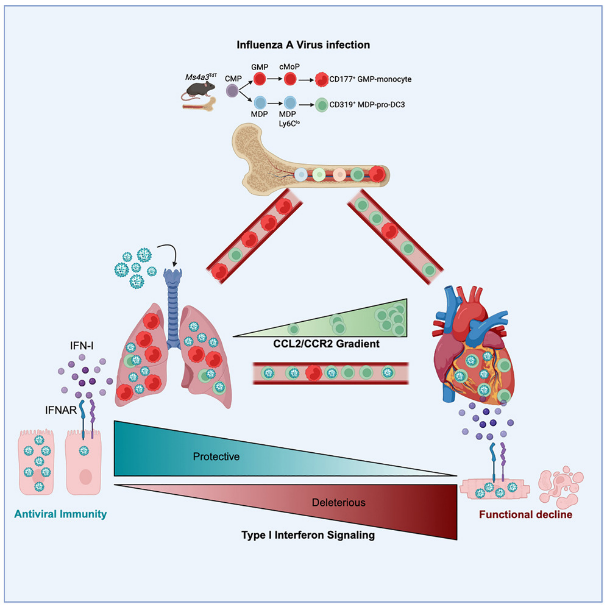
Figura 1. Durante a infecção pulmonar, células mieloides derivadas da medula óssea, especialmente pró-DC3, identificadas por citometria de fluxo como células CD319⁺, entram na circulação após infecção pelo vírus da Influenza A. A expressão de CD319 (SLAMF7) foi utilizada como marcador fenotípico para distinguir essa população mieloide atípica das células CD177⁺, associadas a monócitos clássicos. Guiadas pelo gradiente CCL2-CCR2, essas células pró-DC3 migram para o miocárdio e transferem o vírus da Influenza A aos cardiomiócitos. Essa infecção desencadeia uma resposta local de interferon tipo I (IFN-I). Embora a sinalização por IFN-I seja protetora no pulmão, sua ativação no coração contribui para inflamação e disfunção do miocárdio, resultando em lesão cardíaca.
Referências
- DOWNEY, Jeffrey et al. Influenza hijacks myeloid cells to inflict type-I interferon-fueled damage in the heart. Immunity, v. 59, n. 3, p. 637–650.e12, 2026. doi: https://doi.org/10.1016/j.immuni.2025.12.011
- KWONG, Jeffrey C. et al. Acute myocardial infarction after laboratory-confirmed influenza infection. New England Journal of Medicine, v. 378, n. 4, p. 345–353, 2018. doi: https://doi.org/10.1056/NEJMc1805679

- Apaixonados por Imunologia
- Comunicado
- Conteúdo Publicitário
- Curso
- Dept. Imunologia Clínica
- Dia da Imunologia
- Dia Internacional da Imunologia
- Divulgação científica
- Edital
- Especial
- Especial Dia da Imunologia
- Especial Doença de Chagas
- Evento
- Eventos
- Exposição COVID-19 da SBI
- História da Imunologia no Brasil
- Homenagem
- Immuno 2018
- Immuno2019
- Immuno2021
- Immuno2022
- Immuno2023
- Immuno2025
- Immuno2026
- IMMUNOLAC
- Immunometabolism2022
- Imune
- Imune - o podcast da SBI
- ImunoWebinar
- INCT Imuno
- Institucional
- IUIS
- Luto
- NeuroImmunology 2024
- Nota
- Nota Técnica
- Notícia
- o podcast da SBI
- Oportunidades
- Outros
- Parecer Científico
- Pesquisa
- Pint of Science 2019
- Pint of Science 2020
- Política Científica
- Sars-CoV-2
- SBI 50 ANOS
- SBI.ImunoTalks
- Sem categoria
- Simpósio
- SNCT 2020
- SNCT 2022
- Webinar
- WORKSHOP
.png)