Autores: Jonatan Carvalho e Pietra Buratto
Editora: Profa. Vanessa Carregaro
Seminário apresentado na disciplina Tópicos Avançados de Imunologia do Programa de Pós-Graduação em Imunologia Básica e Aplicada da FMRP-USP.
Um estudo recente, intitulado “Sensory neuron production of substance P and TAFA4 promotes disease tolerance during viral infection”, publicado na revista Immunity em março de 2026 por Anais Roger e colaboradores, traz avanços importantes ao revelar que neurônios sensoriais desempenham um papel ativo na regulação da resposta imune durante infecções virais, promovendo tolerância à doença sem interferir na eliminação do vírus.
A resposta do hospedeiro a infecções é tradicionalmente associada à capacidade de eliminar o patógeno. No entanto, essa resposta pode gerar lesões significativas nos tecidos devido à inflamação exacerbada. Nesse contexto, o conceito de tolerância à doença surge como um mecanismo complementar, no qual o organismo limita as lesões causadas pela infecção sem interferir na carga viral (1). Apesar de avanços na compreensão da imunidade antiviral, os mecanismos pelos quais o sistema nervoso contribui para esse processo ainda permanecem pouco explorados (2).
Para investigar essa interação, os autores utilizaram um modelo murino de infecção cutânea pelo vírus herpes simplex tipo 1 (HSV-1), que apresenta duas fases principais: replicação viral na pele e posterior infecção dos neurônios sensoriais nos gânglios da raiz dorsal (DRGs). Assim, esse modelo permite analisar simultaneamente respostas imunes em tecidos periféricos e no sistema nervoso.
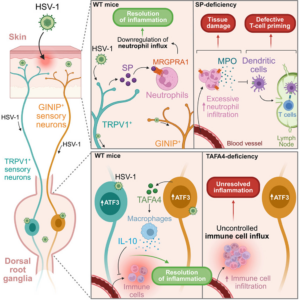
O estudo mostra que o HSV-1 é capaz de infectar neurônios sensoriais, principalmente os neurônios desmielinizados, incluindo as subpopulações neuronais TRPV1⁺ e GINIP⁺. A infecção promove a indução da expressão do fator de transcrição ATF3, um marcador de estresse neuronal. Como consequência, os neurônios passam a exercer funções imunomoduladoras, a fim de prevenir a lesão tecidual, destacando-se a liberação de substância P (SP) e da neurocina TAFA4. Essas moléculas atuam na regulação da resposta inflamatória, tanto na pele, quanto nos DRGs, mas não influenciam nos mecanismos de eliminação viral.
Nos DRGs, a ausência de TAFA4, explorada por meio de engenharia genética animal, mostraram um aumento significativo do infiltrado inflamatório, incluindo monócitos, macrófagos e neutrófilos, após a infecção por HSV-1. Esse fenômeno foi associado à redução de IL-10, uma citocina anti-inflamatória. O estudo mostrou que a principal célula produtora dessa IL-10 no microambiente inflamatório é o macrófago. O bloqueio dessa citocina em animais saudáveis apresentou os mesmos efeitos que a deficiência de TAFA4, aumentando o recrutamento de infiltrado inflamatório para os DRGs. Descata-se que ainda é desconhecido o receptor de TAFA4 responsável pelos efeitos em macrófagos, sendo esse um potencial alvo de estudos futuros. Em contraste, a TAFA4 não apresentou função relevante na pele, evidenciando uma regulação neuroimune altamente dependente do microambiente.
Já no contexto da pele, a SP assume papel central na regulação da resposta inflamatória. Produzida principalmente por neurônios TRPV1⁺, a presença de SP limita o recrutamento excessivo de neutrófilos para o local da infecção. A ausência da produção de SP com bloqueio dos neurônios TRPV1⁺ resultou em maior infiltraçãoneutrofílica, aumento da lesão tecidual e comprometimento da resposta imune adaptativa, com redução da ativação de células dendríticas e da expansão de linfócitos TCD8⁺. Do ponto de vista mecanístico, a SP atua sobre neutrófilos por meio do receptor MRGPRA1, inibindo sua migração, mesmo frente à estimulos quimiotáticos, como CXCL1.
O estudo buscou elucidar por qual mecanismo o infiltrado de neutrófilos intensifica a lesão tecidual. Nessa busca, foi visto que, após a infecção viral, a ausência de substância P provocou um aumento nos níveis de mieloperoxidase (MPO), um dos mediadores liberados por neutrófilos. A inibição da MPO foi capaz de restaurar a resposta de células TCD8⁺, mesmo sem reduzir a inflamação local, indicando que neutrófilos em excesso comprometem diretamente a imunidade.
Em conjunto, os dados revelam dois eixos neuroimunes complementares, TAFA4–IL-10 nos DRGs e SP–MRGPRA1 na pele, promovendo assim, tolerância à doença ao limitar a inflamação sem interferir no controle viral, destacando o sistema nervoso como regulador ativo da resposta imune. Esses resultados podem auxiliar na compreensão da razão pela qual a percepção de dor e gravidade da doença causada pela infecção por HSV-1 é indivíduo-específica, visto que a liberação desses mediadores de tolerância também varia entre indivíduos.
Figura 1. Durante a infecção cutânea por HSV-1, neurônios sensoriais TRPV1⁺ e GINIP⁺ são ativados e induzem expressão de ATF3. Na pele, neurônios TRPV1⁺ produzem SP, que atua em neutrófilos via receptor MRGPRA1, reduzindo sua migração e promovendo resolução da inflamação. Na ausência dessa via, há infiltração excessiva de neutrófilos, aumento de MPO e prejuízo na ativação de células dendríticas e linfócitos T. Nos DRGs, os neurônios produzem TAFA4, que por sua vez induz IL-10 em células mieloides e controla a inflamação. A deficiência de TAFA4 resulta em inflamação persistente, sem alterar a carga viral. Assim, os eixos SP–MRGPRA1 (pele) e TAFA4–IL-10 (DRG) promovem tolerância à doença ao limitar o dano tecidual sem comprometer a resposta antiviral.
Referências
1 - Roger A, Reynders A, Hoeffel G, Ugolini S. Neuroimmune crosstalk in the skin: a delicate balance governing inflammatory processes. Curr Opin Immunol. 2022;77:102212. doi:10.1016/j.coi.2022.102212;
2 - Filtjens J, Roger A, Quatrini L, et al. Nociceptive sensory neurons promote CD8 T cell responses to HSV-1 infection. Nat Commun. 2021;12:2936. doi:10.1038/s41467-021-22841-6.


- Apaixonados por Imunologia
- Comunicado
- Conteúdo Publicitário
- Curso
- Dept. Imunologia Clínica
- Dia da Imunologia
- Dia Internacional da Imunologia
- Divulgação científica
- Edital
- Especial
- Especial Dia da Imunologia
- Especial Doença de Chagas
- Evento
- Eventos
- Exposição COVID-19 da SBI
- História da Imunologia no Brasil
- Homenagem
- Immuno 2018
- Immuno2019
- Immuno2021
- Immuno2022
- Immuno2023
- Immuno2025
- Immuno2026
- IMMUNOLAC
- Immunometabolism2022
- Imune
- Imune - o podcast da SBI
- ImunoWebinar
- INCT Imuno
- Institucional
- IUIS
- Luto
- NeuroImmunology 2024
- Nota
- Nota Técnica
- Notícia
- o podcast da SBI
- Oportunidades
- Outros
- Parecer Científico
- Pesquisa
- Pint of Science 2019
- Pint of Science 2020
- Política Científica
- Sars-CoV-2
- SBI 50 ANOS
- SBI.ImunoTalks
- Sem categoria
- Simpósio
- SNCT 2020
- SNCT 2022
- Webinar
- WORKSHOP
.png)