Autores: Ana Carolina Carvalho e Gabriélly Trindade
Editor: Prof. Dr. Marco Ataide
Seminário apresentado na disciplina Tópicos Avançados de Imunologia do Programa de Pós-Graduação em Imunologia Básica e Aplicada da FMRP-USP.
Recentemente, foi publicado no periódico Science Immunology o estudo intitulado “Monocyte-derived IL-10 drives sex differences in pain duration”, no qual Jaewon Sim e colaboradores identificam que a experiência de dor prolongada no sexo biológico feminino está relacionada a diferenças na abundância e na sinalização androgênica de monócitos produtores de IL-10, sugerindo assim alvos potenciais para o tratamento da dor crônica.1
Utilizando um modelo de dor inflamatória induzida por CFA (adjuvante completo de Freund) em camundongos C57BL/6, os autores demonstraram que apesar de quantidades equivalentes de infiltrado inflamatório e edema, a resolução da dor foi mais rápida nos machos, enquanto as fêmeas mantiveram hipersensibilidade mecânica por mais tempo.
Aprofundando as investigações, o grupo identificou que os camundongos machos apresentam maior número de células produtoras de IL-10 na pele inflamada, especificamente no momento da resolução. A administração de IL-10 recombinante diretamente na pele acelerou a resolução da dor em ambos os sexos. A identificação do receptor IL-10R1 em neurônios sensoriais periféricos, aliada à deleção condicional desse receptor especificamente nesses neurônios (modelo Avil-Il10ra), demonstrou que a IL-10 atua diretamente nos neurônios para promover a resolução da dor.
Para identificar a fonte celular da IL-10, os autores utilizaram citometria de fluxo espectral de alta dimensão em camundongos repórteres Il10-GFP. Os monócitos infiltrantes Ly6Chigh foram identificados como a principal população produtora de IL-10. Observou-se que os machos apresentaram uma maior abundância dessa população celular, o que se correlacionou diretamente com a resolução da dor. Além disso, o grupo identificou quatro subpopulações distintas de monócitos, destacando-se o subconjunto CD206high como o mais enriquecido na produção de IL-10 e mais abundante nos camundongos machos.
Utilizando o modelo de depleção de células mieloides por meio da admistração da toxina difitérica em camundongos LysM-DTR, e o modelo de deleção gênica condicional de IL-10 também em células LysM+ (LysM-Il10 cKO) , observou-se um aumento no tempo da resolução da dor. Outras abordagens, como a utilização de camundongos CCR2 KO e a administração de anticorpo anti-CCR2 durante a fase de resolução, confirmaram que a depleção seletiva de monócitos, ou a sua mobilização impede a resolução da dor.
Os hormônios sexuais emergiram como os reguladores centrais dessa via. Em fêmeas, a ovariectomia não alterou a resolução da dor, indicando que os estrógenos não são determinantes. No entanto, a administração de DHT (dihidrotestosterona) em fêmeas ovariectomizadas aumentou os monócitos CD206high produtores de IL-10 e acelerou a resolução da dor. Em machos, a orquiectomia (remoção cirúrgica dos testículos) atrasou a resolução da dor e reduziu os monócitos IL-10+, enquanto o bloqueio farmacológico do receptor de andrógeno com flutamida ou a deleção genética desse receptor especificamente em células mieloides (modelo LysM-Ar KO) reproduziu o mesmo fenótipo de dor prolongada.
Por fim, os autores exploraram o potencial terapêutico de modular essa via utilizando resolvina D1 (RvD1), um mediador lipídico pró-resolução derivado do ômega-3. A administração de RvD1 no início da fase de resolução acelerou significativamente a resolução da dor em ambos os sexos. A RvD1 aumentou seletivamente os monócitos CD206high produtores de IL-10, mimetizando o efeito dos andrógenos. Por fim, eles demonstram que em camundongos LysM-Il10 cKO, a RvD1 perdeu completamente seu efeito terapêutico, confirmando que sua ação depende da IL-10 derivada de monócitos.
A validação translacional foi realizada em pacientes com dor pós-trauma. Homens resolveram a dor mais rapidamente do que mulheres, e essa resolução mais rápida foi associada a maiores níveis circulantes de monócitos e IL-10 em homens, corroborando os achados em camundongos.
Em conjunto, os resultados estabelecem um modelo no qual os andrógenos atuam diretamente em monócitos para aumentar especificamente o subconjunto CD206high produtor de IL-10, que por sua vez sinaliza para neurônios sensoriais via IL-10R1, promovendo a resolução da dor. A menor sinalização androgênica em fêmeas explica sua resolução mais lenta. A resolvina D1, ao aumentar esses monócitos independentemente do sexo, emerge como uma estratégia terapêutica promissora para acelerar a resolução da dor e prevenir sua cronificação.
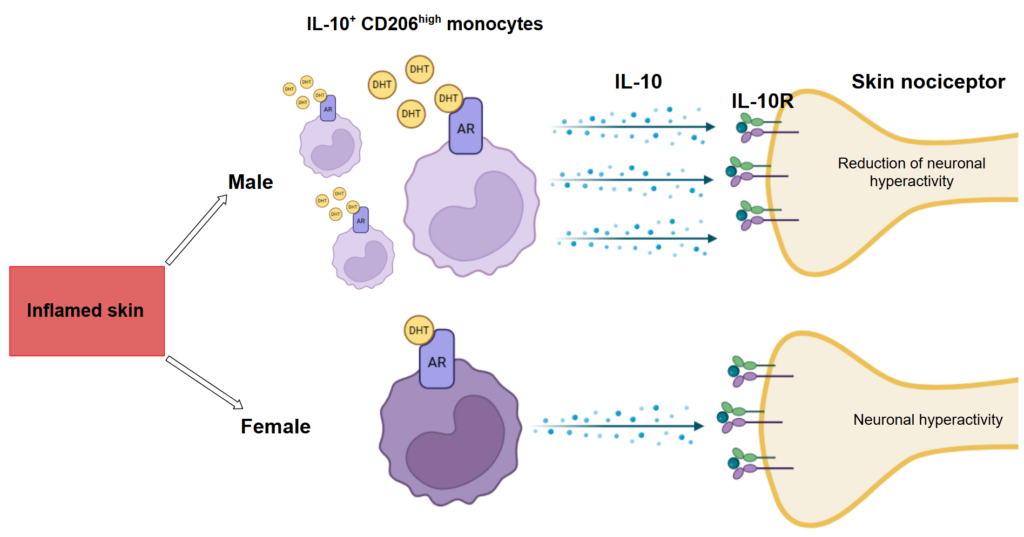
Durante o processo inflamatório na pele de modelos animais machos, a presença e a sinalização do hormônio andrógeno promove um aumento significativo na quantidade de monócitos com o fenótipo CD11bhighLy6ChighCD11clowF4/80low-intSiglecFlowCCR2high, CD163negCD206high. Esses monócitos são responsáveis pela produção elevada de IL-10 que sinaliza através do receptor IL-10R presente nos nociceptores periféricos. Essa sinalização resulta na diminuição da hiperatividade neuronal, levando a uma redução na sensibilidade à dor. Em contraste, nas fêmeas, tanto a quantidade desses monócitos quanto a produção de IL-10 são significativamente reduzidas. Essa diminuição impacta negativamente na regulação da hiperatividade neuronal, resultando em uma maior sensibilidade à dor. Assim, as diferenças sexuais na resposta à dor são atribuídas à disparidade na abundância e na atividade dos monócitos IL-10 produtores entre machos e fêmeas, evidenciando o papel crucial dos andrógenos na modulação da dor inflamatória.
.Referências
- Jaewon Sim et al. ,Monocyte-derived IL-10 drives sex differences in pain duration.Sci. Immunol.11,eadx0292(2026).DOI:10.1126/sciimmunol.adx0292.

- Apaixonados por Imunologia
- Comunicado
- Conteúdo Publicitário
- Curso
- Dept. Imunologia Clínica
- Dia da Imunologia
- Dia Internacional da Imunologia
- Divulgação científica
- Edital
- Especial
- Especial Dia da Imunologia
- Especial Doença de Chagas
- Evento
- Eventos
- Exposição COVID-19 da SBI
- História da Imunologia no Brasil
- Homenagem
- Immuno 2018
- Immuno2019
- Immuno2021
- Immuno2022
- Immuno2023
- Immuno2025
- Immuno2026
- IMMUNOLAC
- Immunometabolism2022
- Imune
- Imune - o podcast da SBI
- ImunoWebinar
- INCT Imuno
- Institucional
- IUIS
- Luto
- NeuroImmunology 2024
- Nota
- Nota Técnica
- Notícia
- o podcast da SBI
- Oportunidades
- Outros
- Parecer Científico
- Pesquisa
- Pint of Science 2019
- Pint of Science 2020
- Política Científica
- Sars-CoV-2
- SBI 50 ANOS
- SBI.ImunoTalks
- Sem categoria
- Simpósio
- SNCT 2020
- SNCT 2022
- Webinar
- WORKSHOP
.png)