Autores: Jackeline Marino e Thaílla Pacheco
Editora: Daniela Carlos Sartori
O artigo científico intitulado “Myelin antigen capture in the CNS by B cells expressing EBV latent membrane protein 1 leads to demyelinating lesion formation”, publicado na revista Cell em janeiro de 2026 por Kim H. et al, traz atualizações sobre o possível mecanismo de envolvimento do Epstein-Barr vírus com a esclerose múltipla, uma doença autoimune crônica e inflamatória do sistema nervoso central (CNS)¹. O vírus Epstein-Barr (EBV), é um herpesvírus humano, agente causador da mononucleose infecciosa, que está presente em cerca de 90% da população mundial². De forma relevante, anticorpos contra EBV estão presentes praticamente em 100% dos pacientes diagnosticados com esclerose múltipla³. A esclerose múltipla é uma doença crônica na qual células imunes autorreativas atacam a proteína mielina, que reveste os neurônios e possibilita a transmissão do impulso nervoso⁴. Um dos mecanismos propostos para a relação entre o EBV e a esclerose múltipla é que células autorreativas infectadas pelo EBV conseguem sobreviver, resultando em falha da tolerância periférica do organismo⁵. Corroborando, a LMP1 (latent membrane protein 1), proteína expressa na membrana em células B com infecção latente de EBV, está relacionada às células B de longa vida⁶. Essa proteína mimetiza um sinal constitutivo de CD40, molécula importante na ativação de células B⁷. Sendo assim, os autores hipotetizaram que células B autorreativas conseguem infiltrar o cérebro, cuja barreira hematoencefálica se torna permeável pela infecção viral, capturar antígeno da mielina e receber sinais de sobrevivência pela infecção por EBV, especificamente com a expressão de LMP1 na membrana.
O estudo demonstrou que linfócitos B naive, incluindo aqueles autorreativos para mielina, são capazes de infiltrar o SNC em contextos inflamatórios e capturar antígenos diretamente do parênquima, independentemente de órgãos linfoides. No entanto, esse reconhecimento antigênico isolado não resulta em ativação patogênica: na ausência de sinais adicionais, esses linfócitos B entram rapidamente em morte induzida por ativação (AICD), caracterizando um mecanismo de tolerância periférica. Mesmo na presença de células T naive específicas, não houve resgate funcional dessas células no SNC, indicando que o ambiente local não favorece a cooperação B–T nesse contexto inicial. A presença de sinais de sobrevivência mais fortes, como CD40L ou a expressão da proteína viral LMP1, mudou o desfecho dessas células. Nessas condições, os linfócitos B que haviam capturado antígeno passaram a sobreviver, proliferar e adquirir função efetora, resultando na formação de lesões desmielinizantes associadas à produção de autoanticorpos e à ativação de células mieloides. A expressão de LMP1, em particular, atuou como um substituto funcional do sinal de ajuda de células T, o CD40L, potencializando a resposta quando combinada ao reconhecimento antigênico. Esses efeitos foram observados tanto em modelos ex vivo quanto in vivo, com evidências de ativação de micróglia e aumento da marcação de componentes do sistema complemento nas áreas lesionadas, sugerindo participação de mecanismos mediados por autoanticorpos na lesão tecidual.
Em conjunto, os achados sugerem que a captura de antígeno por linfócitos B no SNC, por si só, não é suficiente para iniciar a doença, mas pode se tornar patogênica quando associada a sinais de sobrevivência como os induzidos pelo EBV. Esse modelo integra a presença de linfócitos B autorreativos, a infecção por EBV e a formação de lesões desmielinizantes, propondo que a quebra da tolerância periférica ocorre quando essas células escapam da AICD e passam a atuar como efetoras no tecido, por meio da expressão de LMP1. Dessa forma, o estudo fornece uma explicação mecanística para a associação entre EBV e esclerose múltipla e aponta possíveis alvos terapêuticos relacionados à sobrevivência e ativação de linfócitos B no SNC.
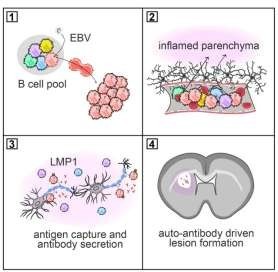
Figura 1. Modelo proposto para o início de lesões desmielinizantes mediadas por linfócitos B no sistema nervoso central (SNC) após infecção por Epstein-Barr. (1) Linfócitos B, incluindo clones autorreativos, podem ser infectados pelo EBV e persistir no repertório como células potencialmente patogênicas. (2) Em contextos inflamatórios, esses linfócitos B infiltram o parênquima cerebral, onde entram em contato direto com antígenos locais.
(3) A expressão de LMP1, proteína viral com função análoga à sinalização via CD40, permite a sobrevivência dessas células após captura antigênica, promovendo sua ativação e secreção de autoanticorpos. (4) Ocorre a formação de lesões desmielinizantes mediadas por autoanticorpos, associadas à inflamação local e dano tecidual.
REFERÊNCIAS:
- Kim H, Schneider M, Sarrat C, Savidan A, Bell B, Schreiner B, et Myelin antigen capture in the CNS by B cells expressing EBV latent membrane protein 1 leads to demyelinating lesion formation. Cell. 2026 Jan 22;189(2):603- 619.e25. doi:10.1016/j.cell.2025.12.031.
- Zanella L, Riquelme I, Buchegger K, Abanto M, Ili C, Brebi P. A reliable Epstein-Barr Virus classification based on phylogenomic and population analyses. Sci Rep. 2019 Jul 8;9(1):9829. doi:10.1038/s41598-019-45986-3.
- Pakpoor J, Disanto G, Gerber JE, Dobson R, Meier UC, Giovannoni G, et al. The risk of developing multiple sclerosis in individuals seronegative for Epstein-Barr virus: a meta-analysis. Mult 2013 Feb;19(2):162-6. doi:10.1177/1352458512449682.
- Comi G, Bar-Or A, Lassmann H, Uccelli A, Hartung HP, Montalban X, et al. Role of B Cells in Multiple Sclerosis and Related Disorders. Ann Neurol. 2021 Jan;89(1):13-23. doi:10.1002/ana.25927.
- Behrens M, Comabella M, Lünemann EBV-specific T-cell immunity: relevance for multiple sclerosis. Front Immunol. 2024 Dec 24;15:1509927. doi:10.3389/fimmu.2024.1509927.
- Price AM, Tourigny JP, Forte E, Salinas RE, Dave SS, Luftig MA. Epstein-Barr virus ensures B cell survival by uniquely modulating apoptosis at early and late times after infection. Elife. 2017 Apr 20;6:e22509. doi:10.7554/eLife.22509.
- Kaye KM, Izumi KM, Kieff E. Epstein-Barr virus latent membrane protein 1 is essential for B-lymphocyte growth transformation. Proc Natl Acad Sci U S A. 1993 Oct 1;90(19):9150-4. doi:10.1073/pnas.90.19.9150.


- Apaixonados por Imunologia
- Comunicado
- Conteúdo Publicitário
- Curso
- Dept. Imunologia Clínica
- Dia da Imunologia
- Dia Internacional da Imunologia
- Divulgação científica
- Edital
- Especial
- Especial Dia da Imunologia
- Especial Doença de Chagas
- Evento
- Eventos
- Exposição COVID-19 da SBI
- História da Imunologia no Brasil
- Homenagem
- Immuno 2018
- Immuno2019
- Immuno2021
- Immuno2022
- Immuno2023
- Immuno2025
- Immuno2026
- IMMUNOLAC
- Immunometabolism2022
- Imune
- Imune - o podcast da SBI
- ImunoWebinar
- INCT Imuno
- Institucional
- IUIS
- Luto
- NeuroImmunology 2024
- Nota
- Nota Técnica
- Notícia
- o podcast da SBI
- Oportunidades
- Outros
- Parecer Científico
- Pesquisa
- Pint of Science 2019
- Pint of Science 2020
- Política Científica
- Sars-CoV-2
- SBI 50 ANOS
- SBI.ImunoTalks
- Sem categoria
- Simpósio
- SNCT 2020
- SNCT 2022
- Webinar
- WORKSHOP
.png)